2022年全国药品申报仍旧呈上涨的趋势,截止12月31日,CDE受理的受理号个数达12244个,较2021年添加了5.85%。本陈述针对重庆市2022年药品申报与审评结束状况做剖析:
2022年CDE受理重庆市注册请求受理号198个(以受理号计,计算申报企业中包括注册地址在重庆市的企业),同比添加8.79%,占全国的受理总量比重的1.62%。除掉弥补请求(一致性点评受理号在外,下同)和进口数据后受理号120个,其间化药106个,中药1个,生物制品13个,总数较2021年添加1个。2018-2022年重庆市药品注册请求受理状况(除掉弥补、进口)详见图1:
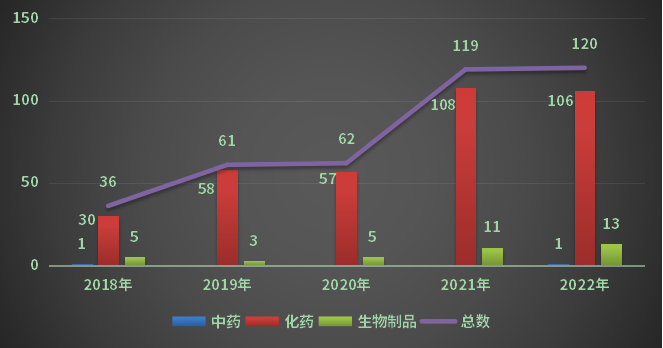
2022年CDE受理重庆市药品以注册请求类别计算,受理新药临床试验请求(以下简称IND)17个受理号,同比削减26.09%;同名同方药、仿制药、生物相似药上市答应请求(以下简称ANDA)受理号71个,同比添加33.96%;仿制药质量和效果一致性点评注册请求(该注册请求类别以下简称一致性点评请求)受理号32个。2018-2022年重庆市各请求类别注册请求受理量详见图2:
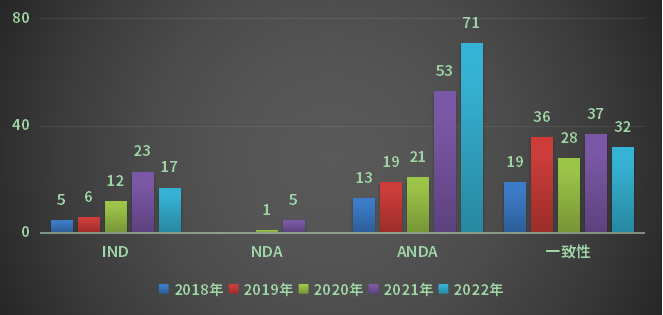
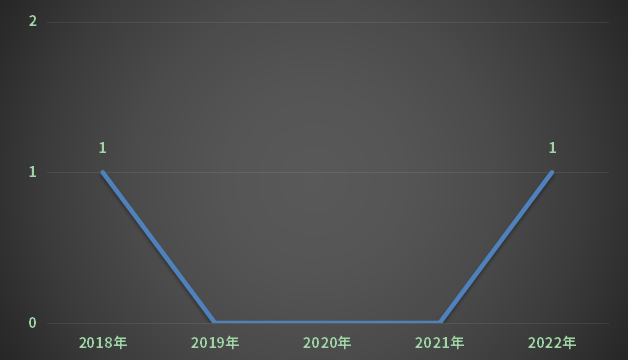
2022年重庆市1类创新药请求受理号10个,其间化药请求3个受理号;生物制品请求6个受理号;中药请求受理号1个。2018-2022年重庆市1类创新药请求受理状况详见图3:
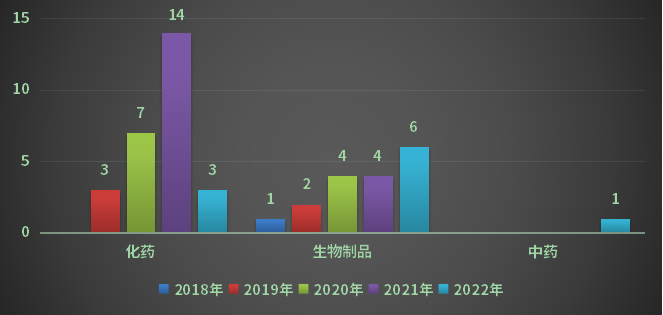
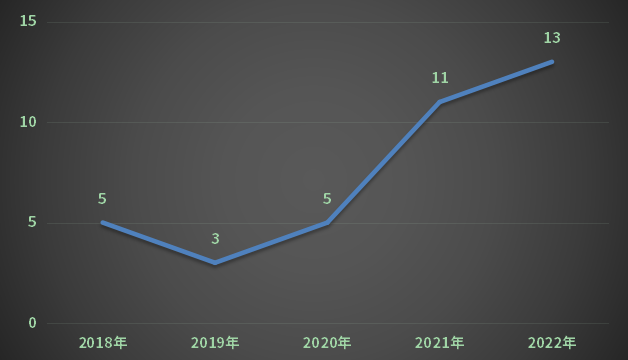
在国内各省市的药品申报方面(依据申报企业注册所在地计算,除掉弥补、进口数据),2022全年申报江苏以884个受理号位居榜首,其间,重庆位居第13;2022年国内各省市申报状况见图4。
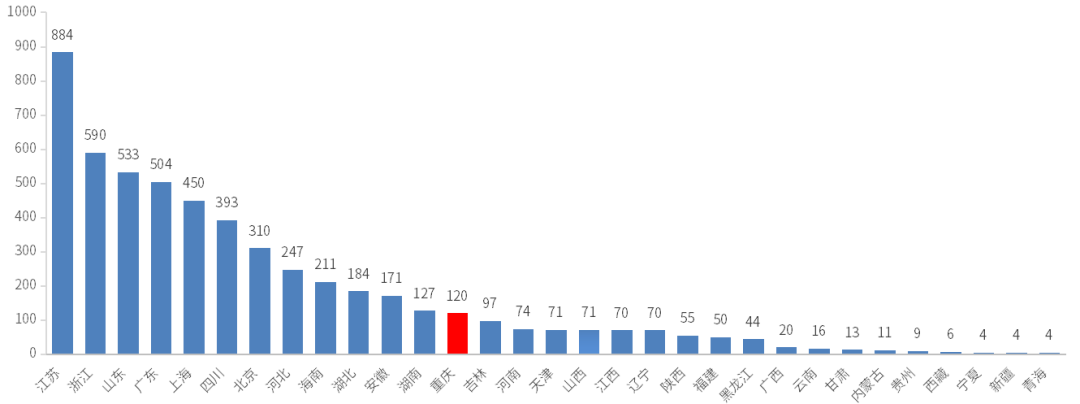
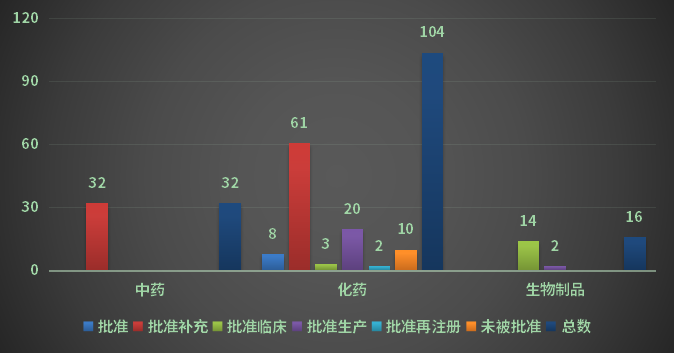
依据药智注册与受理数据库最新计算,重庆市2022年(注:状况开端时刻(药智)从2022年1月1日至2022年12月31日)结束审评受理号158个;药智收录到定论的数量为152个受理号,对有定论的受理号做多元化的剖析计算,其间化药104个,中药32个,生物制品16个。2022年重庆市注册请求审评结束定论概况计算见图5:
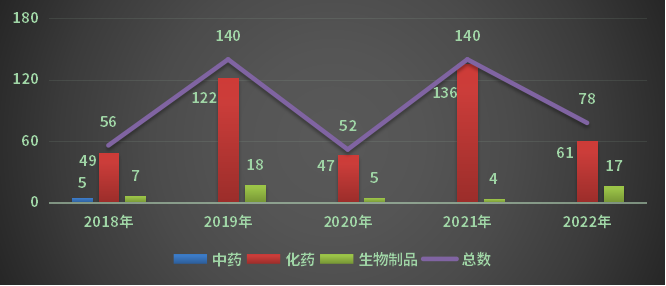
以药品类型计算(除掉弥补、进口),2022年重庆市全年化药结束审评受理号61个;生物制品结束审评受理号17个;2018-2022年重庆市各药品类型注册请求结束审评状况(除掉弥补、进口)见图6。
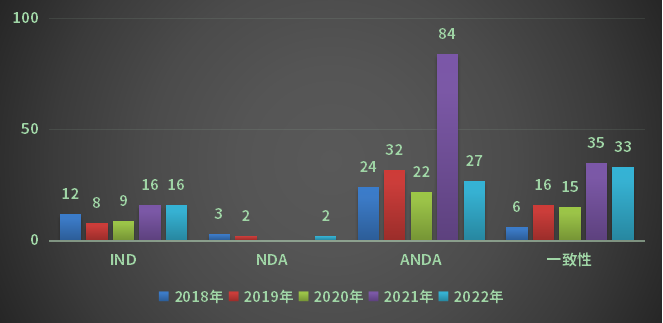
以注册请求类别计算,在2022年重庆市结束审评的受理号中,按审评使命分类,IND请求受理号16个,ANDA请求受理号27个,NDA请求受理号2个,一致性点评受理号有33个。2018-2022年重庆市各审评使命类别审评结束状况详见图7:
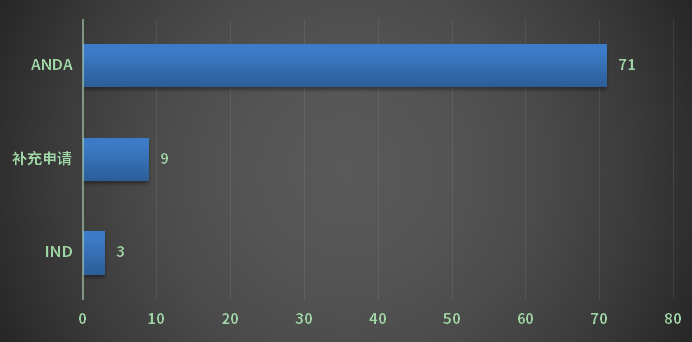
2022年CDE共受理重庆市化学药注册请求受理号147个,以审评使命类别计算,IND请求受理号3个;ANDA请求受理号71个。2022年重庆市化学药各审评使命类别请求受理状况详见图8:
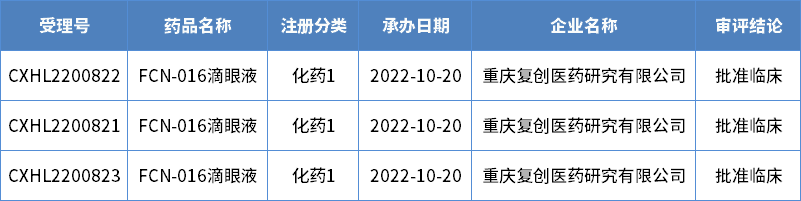
2022年重庆市化药1类申报仅有1个种类,为重庆复创医药研讨有限公司申报的FCN-016滴眼液。2022年重庆市化药1类申报受理状况详见表1。表1 2022年重庆市化药1类申报受理状况
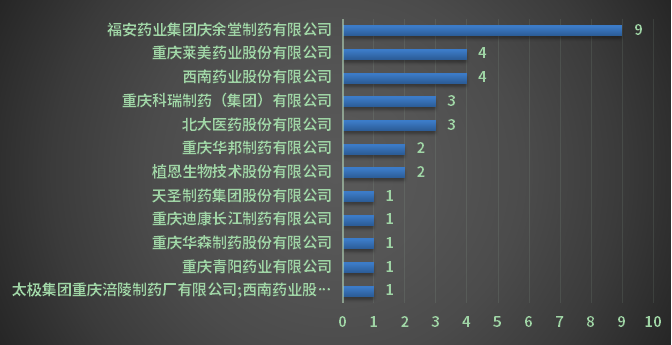
受一致性批件大趋势的影响,2022年重庆市一致性点评受理号申报32个(以受理号计),较2021年削减了5个,占2022年全国一致性点评受理总量的3.83%(如想了解详细状况,请重视药智注册受理数据库)。2022年重庆市各企业一致性点评受理数量详见图9:
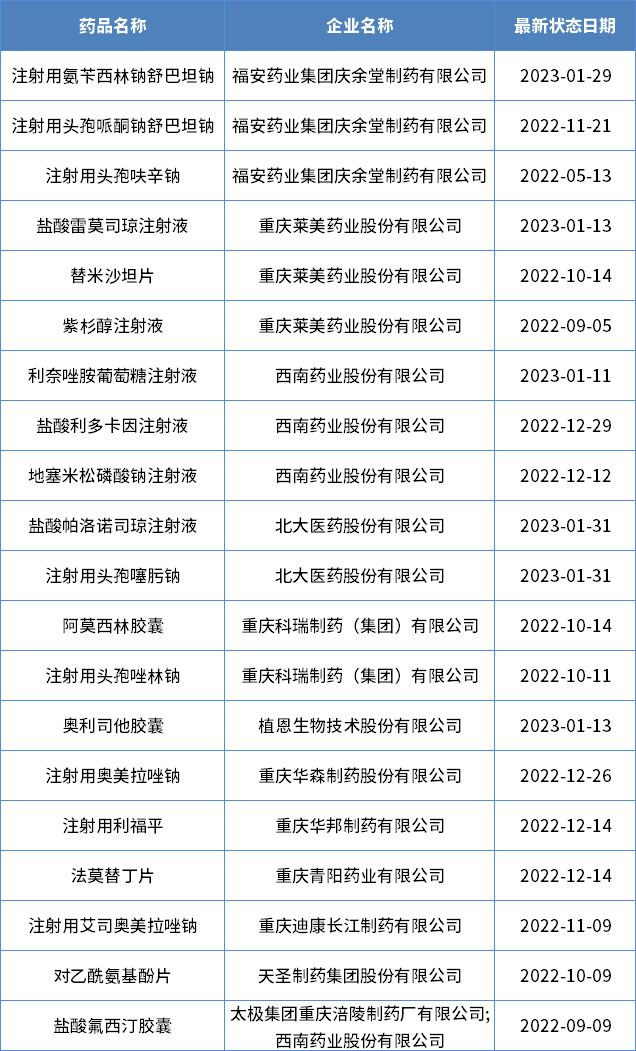
本年度的重庆市化药一致性点评申报排行榜中,福安药业集团庆余堂制药有限公司为榜首,合计申报9个受理号(3个种类)。2022年重庆市一致性点评申报种类受理状况详见表2:
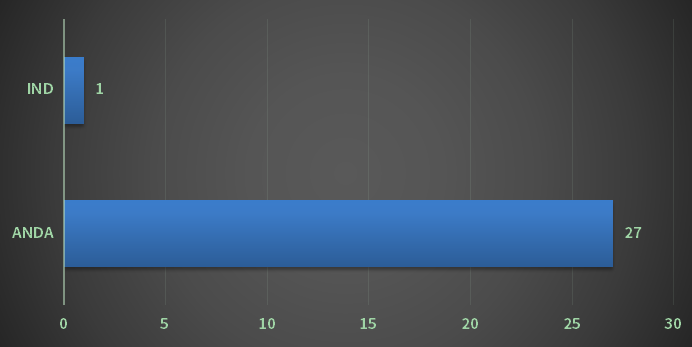
重庆市2022年CDE共结束审评的化学药共106个受理号(包括无需技能审评的受理号),以审评使命类别计算,IND请求1个,ANDA请求27个。2022年重庆市化学药各审评使命类别结束审评状况详见图10:
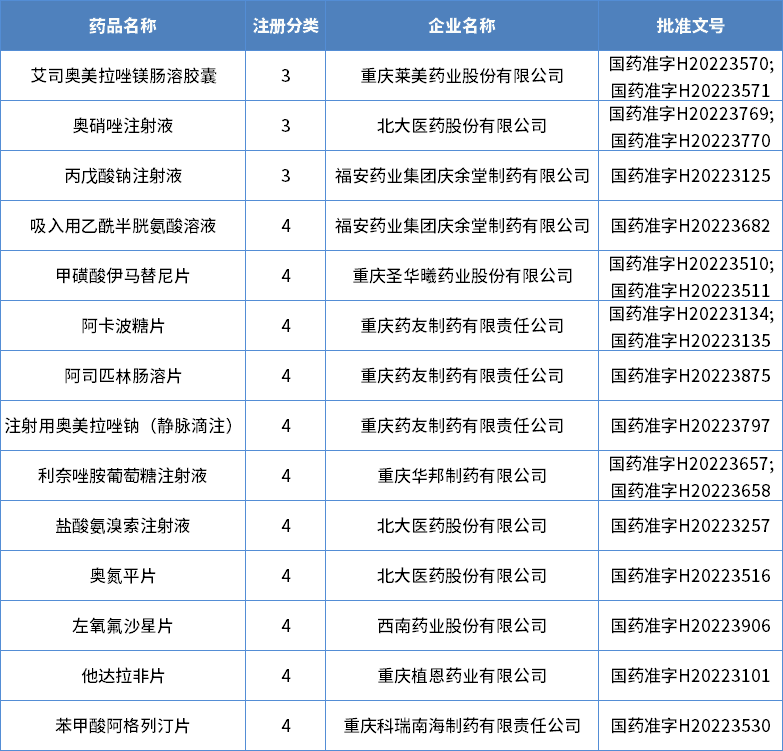
2022年重庆市共15个化药仿制药同意上市(按药品名+企业维度计算),其间注册分类为3类的3个,注册分类4类的11个和注册分类6类的1个。2022年重庆市获批化药仿制药信息状况见表3:表3 2022年重庆市获批化药仿制药信息
2022年CDE承办的重庆市中药注册请求以受理号计共有34个,仅有1个是1.1类新药,为重庆巨琪诺美制药有限公司和北京中医药大学联合申报的苏合颗粒,其他满是弥补请求。2018-2022年重庆市中药受理状况(除掉弥补、进口)详见图11:
在2022年重庆市审评结束中药注册请求受理号33个(包括无需技能审评的受理号),请求类型悉数为弥补请求。
2022年重庆市生物制品共17个受理号获CDE受理,除掉弥补请求和进口数据后受理号13个,按药品类型分类,1个防备用生物制品,12个治疗用生物制品;按审评使命分类,悉数为临床试验请求。2018-2022年重庆市生物制品受理状况(除掉弥补、进口)详见图12:
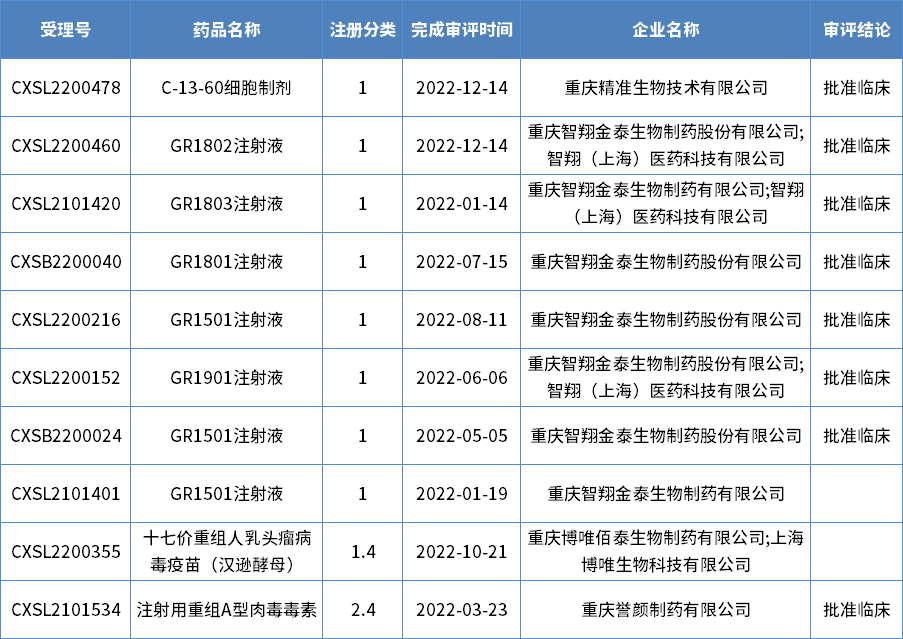
在2022年CDE重庆市审评结束生物制品注册请求受理号19个,以审评使命类别计算,上市请求2个,临床试验请求15个。2022年重庆市生物制品新药结束审评详见表4:表4 2022年重庆市生物制品新药结束审评状况
CDE揭露寻求《发酵或半组成化学仿制药抗生素有关物质极限拟定辅导准则(寻求定见稿)》定见
我国国家药品监督管理局同意备思复(注射用维恩妥尤单抗)用来治疗部分晚期或转移性尿路上皮癌
FDA免除对宜联生物HER3 ADC的1期临床的Partial Hold
浙江微智源能源技能有限公司(化学原料药环保安全技能服务渠道 成员单位)